在前幾篇的介紹中,大家可以感受到日本病理學會 ( The Japanese Society of Pathology, 簡稱 JSP ) 試著在臨床可行的組織擷取以及 FFPE 處理流程下,讓組織內的 DNA / RNA 保有基因檢測的可行性。而此篇是關於 JSP 對樣品的可判讀度、可用度、與定序靈敏度的建議,介紹使用何種 FFPE 切片,紀錄下甚麼資訊,如何評估其 DNA / RNA 可實驗性,搭配適當的 VAF 靈敏度定序,以獲得真正有判讀價值的基因定序結果。
【圖一】臨床樣品處理流程
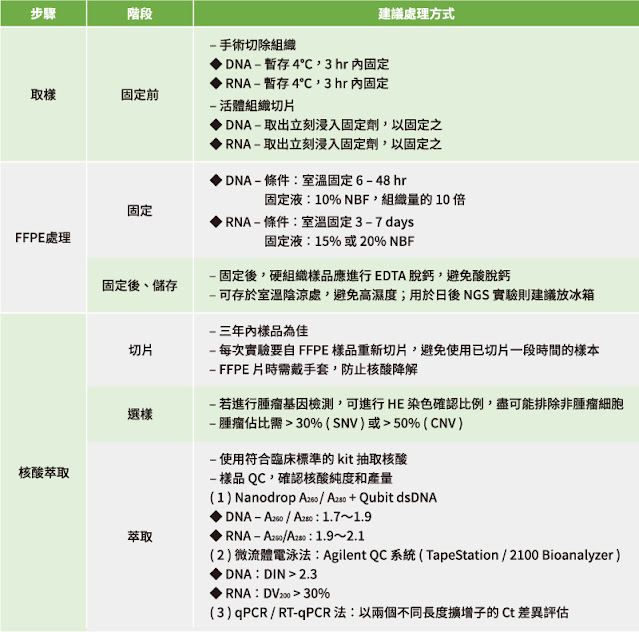
日本病理學會 ( JSP ) 對 FFPE 樣品選擇及核酸萃取建議:
切片、選樣:
每一次核酸萃取前再切新的 FFPE 切片來用,要戴手套執行以避免核酸降解。選樣部分 ( 如圖二 ),若進行腫瘤細胞基因檢測,建議要做 HE 染色並大略紀錄組織腫瘤比率,SNV 分析需要 > 30% 腫瘤比,CNV 分析需要 > 50% 的腫瘤比。腫瘤比率太低者需事先移除非腫瘤部分,以拉高突變存在比例 ( VAF, Variation Allele Frequency )。另外,後續基因定序時,定序倍率要能達到 VAF 5-10% 偵測率。
【圖二】基因診斷用的 HE 染色標本範例 ( A ) 藍線:腫瘤細胞擴散區域。黃線:基因檢測取樣範圍。綠線:需要切除的區域。( B ) 避免使用,儘管有腫瘤細胞但嗜中性球 ( neutrophil ) 很多。( C ) 避免使用,多為非腫瘤細胞,如:漿細胞 ( plasma cell ) 和肌肉層 ( muscle layer ),腫瘤細胞比例低。
萃取:
核酸萃取建議選擇臨床樣品適用的試劑,萃取後必須進行核酸品質鑑定 ( QC ) 確認純度與總量,以評估樣品是否合適進行後續定序實驗。測定方法包含:
① Nanodrop A260/A280 + Qubit
dsDNA:最簡單方便的方法,可估計核酸純度與產率,但對於品質的準確度較低。
- DNA測定要求:A260/A280 : 1.7-1.9
- RNA測定要求:A260/A280 : 1.9-2.1
② 微流體電泳法:Agilent QC 系統 ( TapeStation ( DIN + DV200 ) 及 2100 Bioanalyzer ( DV200 ) ),數位化結果以評估核酸完整度,快速、不汙染,合適臨床應用。
- 核酸品質建議標準:DNA:DIN > 2.3;RNA:DV200 > 30% ( DIN = "DNA Integrity Number ",DV200 = " RNA 大於 200nt 片段比例 ",詳細介紹請看日本病理學會 DNA / RNA 樣品 QC 建議。
③ qPCR / RT-qPCR 法:使用兩個不同長度的擴增子的 Ct 差異來評估反應性,依後續應用需求有不同的 primer 設計及評估做法。
【日本病理學會《基因組醫學病理組織標本處理規定》對於定序樣品處理之建議】
透過 JSP《基因組醫學病理組織標本處理規定》,了解到為將 NGS 納入臨床常規應用,日本醫界建議了:
( 1 ) 標準化 Biopsy / FFPE 固定流程
找出醫療院所可行的標準步驟,於採檢 / 保存時維持檢體的 DNA / RNA 品質。
( 2 ) 標準化選樣與抽取
獲得知道比例、有判讀性、合適品質、足量的 FFPE - DNA / RNA 樣品
( 3 ) 標準化樣品 QC 準則
以簡易指標評估樣品可用性,另外標準化還代表了日常可行性,考量臨床場域的人力、操作、時間、維護、方便性等。
( 4 ) 有判讀效力的定序規格
在一定的腫瘤占比下,搭配 5-10% VAF 靈敏度定序規格,取得有效力的定序數據。
在臨床 NGS QC 標準化下,Agilent TapeStation 系統最貼近臨床樣品 QC 需求,具有不汙染、快速分析、數據化結果方便 QC 判讀標準化。有了 Agilent TapeStation QC 系統的協助,標準化的臨床 NGS 樣品 QC 即能十分輕鬆。基於良好的樣品處理與品質,就能取得有效力的定序結果,此刻 NGS 才真的進入臨床,開啟精準醫學應用。
【圖三】Agilent TapeStation 幫助 NGS 臨床實用化
- Yae Kanai. (2018) The Japanese Society of Pathology Guidelines on the handling of pathological tissue samples for genomic research: Standard operating procedures based on empirical analyses. Pathology International, 68 (2) 63-90.
- 日本病理學會:https://pathology.or.jp/





留言
張貼留言